Lý thuyết sự ăn mòn kim loại: Ăn mòn hóa học và ăn mòn điện hóa
i – Khái niệm
Ăn mòn là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường xung quanh.
- Kết quả: Kim loại bị oxi hóa thành ion dương
- Hiện tượng:
- Giải thích:
- Bản chất của các điện cực phải khác nhau.
- Các điện cực phải tiếp xúc trực tiếp hoặc gián tiếp qua dây dẫn.
- Các điện cực tiếp xúc với dung dịch điện phân.
m → mn+ + ne
ii – loại ăn mòn
Có hai loại ăn mòn kim loại: ăn mòn hóa học và ăn mòn điện hóa
1. Ăn mòn hóa học
Ví dụ – thanh sắt trong nhà máy khí cl2
fe + cl2 → fecl3
⇒ Ăn mòn hóa học là quá trình oxi hóa khử, trong đó êlectron từ kim loại chuyển trực tiếp sang các chất trong môi trường.
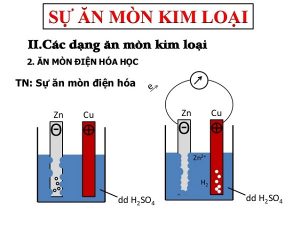
2. Ăn mòn điện hóa
Một. Khái niệm ăn mòn điện hóa
– Kim điện kế quay chỉ báo dòng điện chạy qua.
– Thanh zn bị mòn.
– Bọt khí H2 thoát ra đều ở các thanh cu.

Xem Thêm : Chử Đồng Tử và Công chúa Tiên Dung – Truyện cổ tích
——điện cực âm (a-nốt); zn bị ăn mòn theo phản ứng: zn → zn2+ + 2e
Các ion zn2+ đi vào dung dịch và các electron di chuyển dọc theo dây dẫn đến điện cực đồng.
– Điện cực dương (cathode): Các ion h+ của dung dịch h2so4 nhận electron trở thành nguyên tử h rồi thoát ra thành phân tử h2. : 2h+ + 2e → h2↑
⇒ Ăn mòn điện hóa là quá trình oxi hóa khử, trong đó kim loại bị ăn mòn dưới tác dụng của dung dịch chất điện ly, tạo ra dòng êlectron chuyển dịch từ cực âm sang cực dương.
b. Ăn mòn điện hóa hợp kim sắt trong không khí ẩm
Ví dụ: Gang bị ăn mòn trong không khí ẩm.
– Trong không khí ẩm, trên bề mặt gang luôn có một lớp nước mỏng, lớp nước này hòa tan các khí O2 và CO2 tạo thành dung dịch điện li.
– Sự tiếp xúc của gang có thành phần chủ yếu là fe và c với dung dịch này tạo ra một số pin nhỏ trong đó sắt là cực dương và cacbon là cực âm.
Ở cực dương: fe → fe2+ + 2e
Các electron được giải phóng di chuyển về cực âm.
Ở cực âm: o2 + 2h2o + 4e → 4oh-
Ion Fe2+ hòa tan vào dung dịch điện phân hòa tan trong khí o2, tại đây ion fe2+ tiếp tục bị oxi hóa và dưới tác dụng của ion oh- hình thành gỉ sắt với thành phần chính là fe2o3.nh2o.
c.Điều kiện xảy ra ăn mòn điện hóa
kl – kl cặp; kl – pk; kl – hợp chất
3.Phương pháp chống ăn mòn kim loại
1.Phương pháp bảo vệ bề mặt: sơn, mạ kim loại
2. Phương pháp điện hóa
3. Chế tạo vật liệu không ăn mòn: hợp kim không ăn mòn
Bài tập pin điện hóa và cách giải
Bài 1: Tính thế điện cực chuẩn e0 của cặp oxi hóa khử sau:
A. e0(cr3+/cr), biết suất điện động chuẩn của pin điện hóa cr-ni là +0,51v, e0(ni2+/ni)=-0,23v.
e0(mn2+/mn), biết suất điện động chuẩn của pin điện hóa cd-mn là +0,79v, e0(cd2+/cd)=-0,40v.
Hướng dẫn
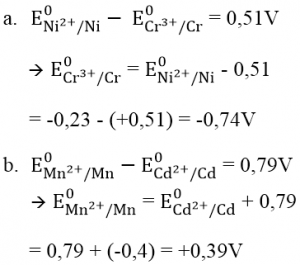
Xem thêm:
Lý thuyết kim loại: Điều chế kim loại
Nguồn: https://xettuyentrungcap.edu.vn
Danh mục: Hỏi Đáp