Mol là gì? Khối lượng Mol là gì? Đơn vị, công thức tính khối lượng mol

Có thể bạn quan tâm
Mole là một trong bảy đơn vị cơ bản của Hệ thống Đo lường Quốc tế, si, được sử dụng trên toàn thế giới. Nốt ruồi là một thuật ngữ thường được nhắc đến trong lĩnh vực hóa học. Vậy hãy xem mol là gì? Khối lượng mol là gì? Bài viết sau đây có đơn vị và công thức tính khối lượng mol là gì:
mol là gì?
Mole, còn được viết là mol, là một đơn vị đo lường được sử dụng trong lĩnh vực hóa học cho các hạt cực nhỏ và mol được sử dụng để mô tả lượng vật chất chứa 6,02214129 (27) × 1023 hạt riêng lẻ. Vị của một nguyên tử hoặc phân tử của một chất.
Số 6,02214129 (27) × 1023, còn được gọi là hằng số Avogadro (ký hiệu n????), không bao giờ thay đổi. Trong phép biến đổi đại lượng hoặc phép tính, ta có thể làm tròn số: n???? = 6,023.1023.
Chúng ta có các ví dụ sau: Ví dụ: 1 mol nguyên tử fe hoặc 6,023.1023 nguyên tử fe.
mol được sử dụng rộng rãi trong hóa học như một cách thuận tiện để biểu thị số lượng chất phản ứng và sản phẩm của một phản ứng hóa học.

Ví dụ ta có phương trình hóa học sau:
2h2 + o2 → 2h2o
Vì vậy, chúng ta có thể hiểu rằng đối với 2 mol hydro (h2) và 1 mol oxy (o2), phản ứng hóa học sẽ tạo thành 2 mol nước (h2o).
mol cũng được sử dụng để biểu thị số nguyên tử, ion hoặc các thực thể khác trong một mẫu vật chất nhất định. Nồng độ của dung dịch được biểu thị bằng mol, được định nghĩa là lượng chất tan hòa tan trong dung dịch trên một đơn vị thể tích, và đơn vị thông thường là mol trên lít (mol / l).
Phân loại số mol nguyên tử và số mol phân tử
Xem Thêm : Soạn văn 12: Nghị luận về một bài thơ, đoạn thơ – Toploigiai
Nguyên tử, phân tử là những hạt vật chất có kích thước siêu nhỏ. Chúng rất nhỏ nên chúng ta không thể nhìn thấy bằng mắt thường. Do đó không thể áp dụng đơn vị đo các hạt vĩ mô (các hạt có thể nhìn thấy bằng mắt thường) cho chúng. Đó là lý do tại sao các nhà khoa học đã đưa ra một đơn vị đo lường mới cho những hạt siêu nhỏ này, đó là nốt ruồi, và đó là lý do tại sao chúng ta có đơn vị là nốt ruồi.
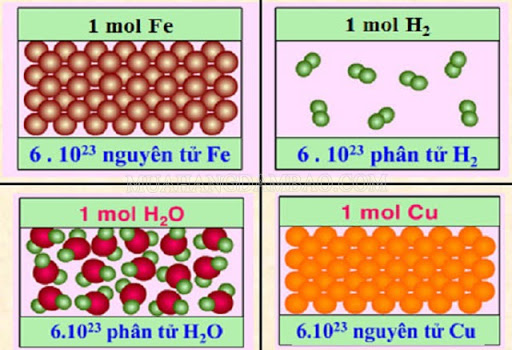
Tuy đều là những hạt vi mô siêu nhỏ nhưng nguyên tử và phân tử lại không giống nhau có lẽ vì thế khái niệm mol nguyên tử và mol phân tử là hai khái niệu hoàn toàn riêng biệt.
- Phân tử của một nguyên tố là số lượng nguyên tử na trong nguyên tố có chứa nguyên tố đó.
- Phân tử của một chất là lượng chất có chứa na phân tử của chất đó. Ở đó.
Chúng tôi có một ví dụ:
- 1 mol nguyên tử oxy sẽ chứa 6,022. 1023 nguyên tử oxy.
- 1 mol o2 oxy sẽ chứa 6,022.1023 phân tử o2
Khối lượng mol là gì?
Định nghĩa khối lượng mol của một chất là gì?
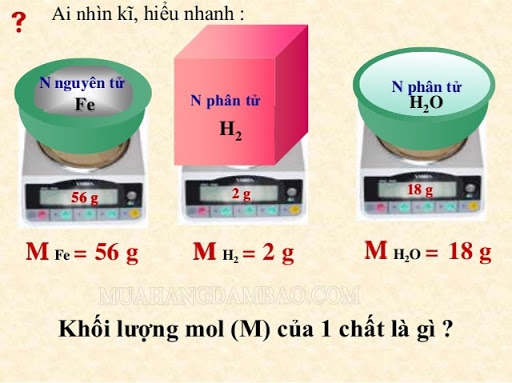
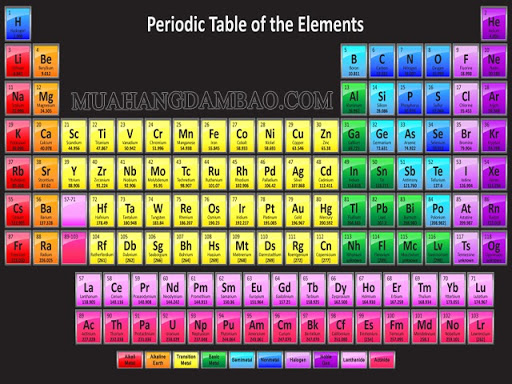
Khối lượng mol của một chất là khối lượng của một mol nguyên tử hoặc phân tử, tính bằng m, gam và bằng khối lượng nguyên tử hoặc khối lượng phân tử của chất đó. Khối lượng mol nguyên tử là khối lượng nguyên tử của nguyên tố trong bảng tuần hoàn.

Ta có ví dụ sau:
- Khối lượng mol của 1 nguyên tử oxy: m (o) = 16g
- Khối lượng mol của 1 nguyên tử hydro: m (h) = 1g
- Khối lượng mol của 1 nguyên tử nước phân tử (h շ o): m (h շ o) = 16 + 2.1 = 18g
Công thức tính khối lượng mol của một chất
Vị trí:
- m là khối lượng mol của chất (tính theo khối lượng nguyên tử hoặc phân tử của chất), tính bằng g / mol.
- m là khối lượng của chất đó tính bằng gam (g).
- n là số mol của chất, tính bằng mol.
Tuy nhiên, công thức trên thường được sử dụng để tính khối lượng của một chất hoặc số mol của chất đó, khối lượng mol bằng khối lượng mol mà chúng ta có thể tìm thấy trong bảng tuần hoàn các nguyên tố hóa học. Hoặc công thức trên, chứng minh chất đó là chất gì sau khi tính khối lượng mol của chất đó.
Khối lượng mol của một số chất:
- Khối lượng mol của không khí: m Không khí là 29 mol / g
- Khối lượng mol của ag: m (ag) = 47 (g)
- Khối lượng mol của bari : m (ba) = 56 (g)
- Khối lượng mol của iot: m (i) = 53 (g)
- Khối lượng mol của Kali: m (k) = 19 ( g)
- Khối lượng mol nitơ: m (n) = 7 (g)
Thể tích mol của chất khí có công thức như thế nào?
Định nghĩa về thể tích mol của một chất khí là gì?
Thể tích mol của một chất khí là thể tích của 1 mol phân tử khí. Hay nói một cách đơn giản, thể tích mol của một chất khí là thể tích do n???? phân tử chất đó chiếm giữ.
Một mol khí bất kỳ có cùng thể tích trong cùng một không gian, ở cùng điều kiện nhiệt độ và áp suất. Theo quy ước, 1 mol khí bất kỳ có thể tích là 22,4 lít ở t = 0 ° c và p = 1 atm (điều kiện tiêu chuẩn).
Xem Thêm : Module là gì? Giải thích Module trong các lĩnh vực
Chúng ta có một ví dụ sau: Ví dụ, sau khi 1 mol khí h շ hoặc 1 mol khí o շ hoặc bất kỳ khí nào khác, nó chiếm thể tích 22,4 lít.
Công thức tính số mol khí ở điều kiện tiêu chuẩn (dktc)
Để tính số mol khí (dktc) theo thể tích, ta có công thức sau:
Khi biết thể tích của khí (đã được xác định), hãy tính số mol của khí đó:
Từ đó, khi biết số mol, ta có công thức tính thể tích khí (dktc): v = n.22,4 (lít)
Vị trí:
- n: số mol của khí (mol)
- v: thể tích của khí ở điều kiện tiêu chuẩn (lít)
Đối với các khí trong điều kiện tự nhiên (điều kiện không tiêu chuẩn), công thức này không còn áp dụng cho các tính toán nữa. Ta sử dụng công thức sau để tính số mol khí ở điều kiện không tiêu chuẩn:
Chúng tôi có:
- p là áp suất (atm)
- v là thể tích khí (lít)
- r = 0,082
- t = 273+ độ Độ C.
Nồng độ mol là gì?
Nồng độ mol được biểu thị bằng m hoặc mol; nó biểu thị số mol chất tan có trong 1 lít dung dịch. Nồng độ mol là phần trăm chất tan được hòa tan trong dung dịch
c% = mct. mdd .100%
Bao gồm:
- c là nồng độ phần trăm của dung dịch, tính bằng%;
- mct là lượng chất tan, tính bằng gam;
- mdd tính bằng gam chất lượng dung dịch.
Trên đây là những kiến thức tổng quát nhất về độ mol mà bạn mua được đảm bảo, hy vọng qua bài viết bạn có thể hiểu được độ mol là gì? Khối lượng mol là gì? đơn vị, công thức tính khối lượng mol và các kiến thức khác có liên quan. Tôi hy vọng bạn đã giải đáp được thắc mắc của mình và có thể áp dụng vào học tập và công việc của mình.
Nguồn: https://xettuyentrungcap.edu.vn
Danh mục: Hỏi Đáp


