Axit Clohidric là gì? Tính chất, cách điều chế, ứng dụng & lưu ý khi dùng

Có thể bạn quan tâm
- Luật Tie-break trong tennis các tay vợt cần biết | Quà Việt
- Lô chẵn lô lẻ chứng khoán là gì? Cách giao dịch lô chứng khoán | Yuanta Yuanta Việt Nam – Tập đoàn tài chính chứng khoán hàng đầu Châu Á
- Cách đặt tên Hán Việt cho con trai và con gái hay nhất 2022
- Phạm Ngũ Lão và bài thơ Tỏ lòng (Thuật hoài) | THPT Sơn Tây
- Bình luận Tên đệm hay cho tên Tuấn ý nghĩa – Tiên Kiếm
Axit clohydric là gì? Cấu trúc phân tử của axit clohydric là gì? Axit clohydric có những tính chất hóa lý nào? Axit clohiđric được điều chế như thế nào? Những ứng dụng nổi bật của axit clohidric và địa chỉ mua axit clohydric chất lượng cao uy tín tại TPHCM ở đâu?
Bạn có biết? Cùng với axit sunfuric, axit clohydric là hóa chất chính, được mệnh danh là “vua của hóa chất” và được sử dụng làm nguyên liệu, vật liệu chính hoặc chất xúc tác trong nhiều ngành sản xuất. Ở bài trước, chúng ta đã tìm hiểu về axit sunfuric. Và hôm nay công ty Zhongshan đã trở lại với một bài viết mới về một chất khác là axit clohydric.
Khi chúng tôi bắt đầu khái niệm đầu tiên của mình Axit clohydric là gì?
Axit clohydric là gì? Cấu trúc phân tử của hcl
Axit clohydric là gì?

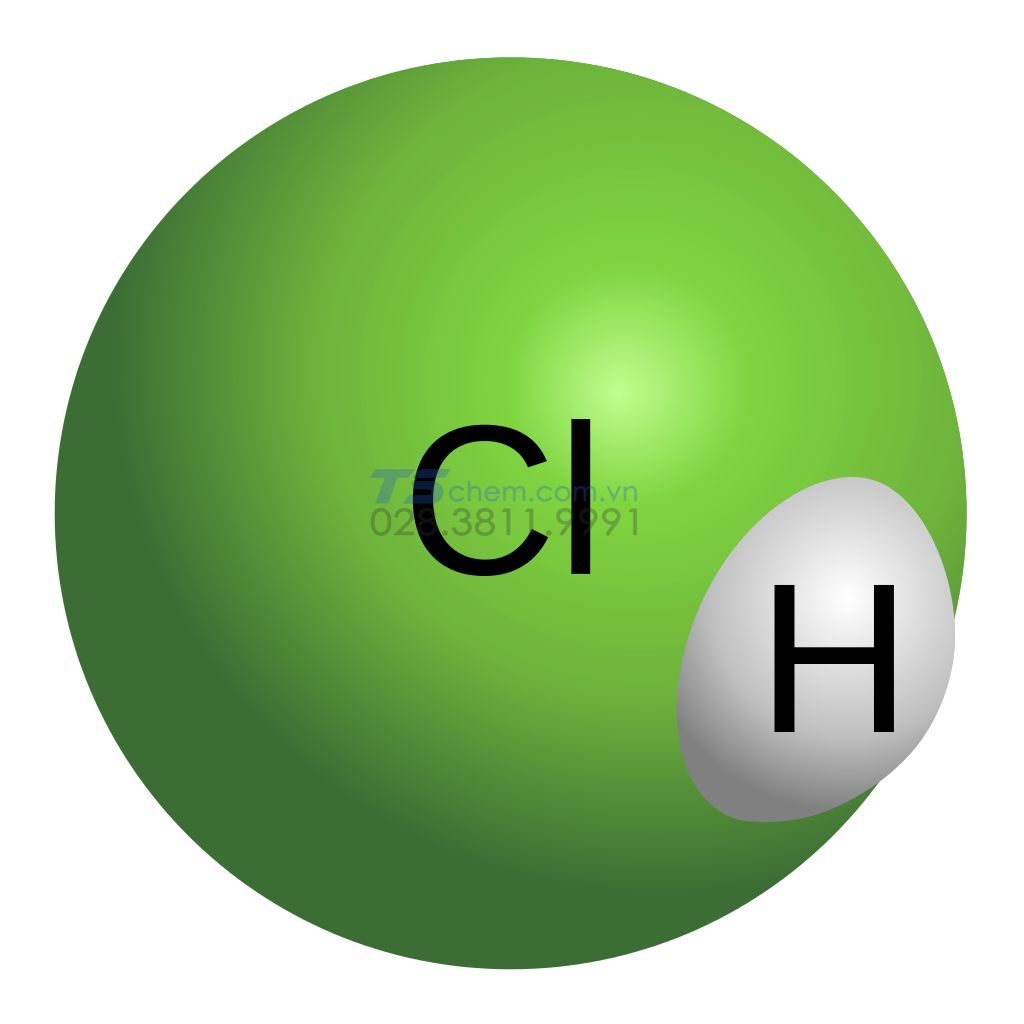
Axit Clohidric là một hợp chất vô cơ có tính axit mạnh. Nó tồn tại ở 2 dạng đó là lỏng và khí. Axit Clohidric có công thức hóa học là HCL và có các tên gọi khác như Axit clohyđric, Axit hiđrocloric, Axit muriatic, Cloran.
axit hcl là một loại axit được sử dụng trong công thức của các ngành công nghiệp dược phẩm, hóa chất và dược phẩm và các chế phẩm, …
Tuy nhiên, hcl ăn mòn các mô của con người, gây tổn thương các cơ quan hô hấp, mắt, da và ruột.
Công thức cấu tạo phân tử của axit clohiđric là gì?
TÍNH CHẤT LÝ HÓA CỦA HCL

Tính chất vật lý của HCL
-
- Hcl là chất khí, không màu, mùi hắc, dễ tan trong nước tạo thành dung dịch axit mạnh, hcl; nặng hơn không khí.
- Là dung dịch axit clohydric loãng không màu, nồng độ axit clohydric đậm đặc nhất có thể lên tới 40% và có màu vàng xanh. Axit này tạo thành sương mù axit ở trạng thái đậm đặc.
- Độ hòa tan trong nước: 725 g / l ở 20 ° c.
- Khối lượng phân tử: 36,5 g / mol.
- hcl là một dung dịch không cháy nhưng dễ bay hơi.
Tính chất hóa học của axit clohydric
Thay đổi màu chỉ thị màu.
-
- Cho giấy quỳ tím vào dung dịch hcl, ta thấy giấy quỳ tím chuyển sang màu đỏ. Đây là một trong những dấu hiệu dùng để nhận biết axit clohiđric.
Axit clohydric phản ứng với bazơ để tạo thành muối và nước.
-
- cu (oh) 2 + 2hcl → cucl2 + 2h2o
- al (oh) 3 + 3hcl → alcl3 + 3h2o
Hcl phản ứng với oxit kim loại để tạo thành muối và sản phẩm của nước, có tính chất của kim loại duy trì hóa trị của chúng.
-
- fe3o4 + 8hcl → 4h2o + fecl2 + 2fecl3
- cuo + 2hcl → cucl2 + h2o
Xem Thêm : Gợi ý 13 cách đặt biệt danh hay, đáng yêu và cực ngộ nghĩnh cho
hcl phản ứng với các kim loại đứng trước h trong dãy phản ứng (trừ pb) để tạo thành muối và giải phóng hiđro.
-
- fe + 2hcl → fecl2 + h2
Axit clohydric phản ứng với muối để tạo thành muối mới và axit mới.
-
- na2co3 + 2hcl → 2nacl + h2o + co2
- agno3 + hcl → agcl + hno3
hcl vừa có tính oxi hóa vừa có tính khử
Tính oxi hóa được thể hiện khi hcl phản ứng với các kim loại đứng trước h2.
-
- mgo + 2h + 1cl → fe + 2cl2 + h20
Phản ứng khử xảy ra khi hcl phản ứng với chất oxy hóa mạnh (như kmno4, k2cr2o7, mno2, kclo3 …)
-
- 2kmn + 7o4 + 16h + 1cl → 2kcl + 2mn + 2cl2 + 5cl20 + 6h2o.
Tham khảo bài viết: znso4 là gì? Tính chất vật lý và hóa học, cách chuẩn bị, hành động và lưu ý khi sử dụng
điều chế hcl
Trong phòng thí nghiệm:
Nồng độ của hcl được điều chế bằng phương pháp axit sunfuric có thể đạt tới 40%, và phương trình điều chế như sau:
-
- rắn nacl + rắn h2so4 → nahso4 + hcl (<2500c)
- 2nacl rắn + rắn h2so4 → na2so4 + 2hcl (> 4000c)
Ngành:
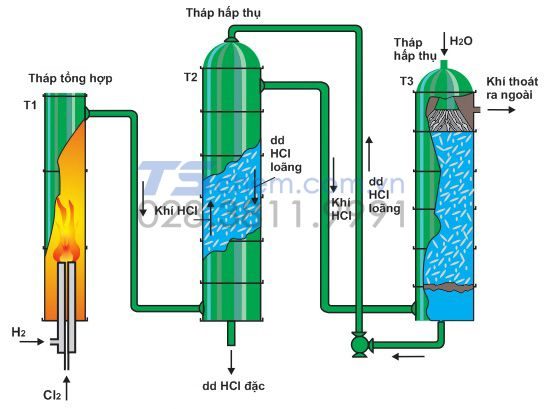
Điều chế HCL bằng phương pháp tổng hợp HCL trong công nghiệp thường được điều chế ở nồng độ phần trăm là 32 -34 % bằng phương pháp tổng hợp với phương trình điều chế sau:
-
- h2 + cl2 → 2hcl (đun nóng)
Ứng dụng của axit clohydric

Ứng dụng của HCL – Dùng Axit HCL để tẩy gỉ thép để loại bỏ gỉ trên thép bằng nồng độ Axit HCL 18% là phổ biến.
-
- fe2o3 + fe + 6 hcl → 3 fecl2 + 3 h2o
– Sử dụng axit clohydric để sản xuất các hợp chất hữu cơ như vinyl clorua và dicloetan để sản xuất pvc hoặc than hoạt tính.
-
- 2 ch2 = ch2 + 4 hcl + o2 → 2 clch2ch2cl + 2 h2o
- gỗ + hcl + nhiệt → than hoạt tính
– Sử dụng axit clohiđric để tạo ra các hợp chất vô cơ thông qua phản ứng axit-bazơ, tạo ra các hợp chất vô cơ. Chất đông tụ và chất đông tụ được sử dụng làm thành phần kết tủa trong xử lý nước thải, sản xuất nước uống, sản xuất giấy hoặc mạ điện, và kẽm clorua trong các ngành công nghiệp mạ điện và sản xuất pin.
Xem Thêm : Soạn bài Nói quá | Soạn văn 8 hay nhất – VietJack.com
– Sử dụng axit clohydric để kiểm soát và trung hòa độ pH, đặc biệt là để điều chỉnh độ kiềm của dung dịch. oh− + hcl → h2o + cl−
– Được tái sinh bằng cách trao đổi ion sử dụng axit clohydric. Axit clohydric này được sử dụng để rửa các cation khỏi nhựa, tạo ra nước khử khoáng. Việc sử dụng này phù hợp với tất cả các ngành công nghiệp hóa chất, sản xuất nước uống và một số ngành công nghiệp thực phẩm.
– Sử dụng axit clohydric trong cơ thể sống: Axit clohydric có trong axit dịch vị do dạ dày tiết ra tạo ra môi trường axit trong dạ dày với độ pH dao động từ 1 đến 2.
– Nhiều phản ứng hóa học liên quan đến axit clohydric được sử dụng trong sản xuất thực phẩm, nguyên liệu thực phẩm và phụ gia thực phẩm. Các sản phẩm đặc biệt như aspartame, fructose, axit citric, lysine, protein thực vật thủy phân và để sản xuất gelatin.
– Ngoài ra, axit clohiđric còn có các công dụng khác như xử lý đồ da, làm sạch nhà cửa và xây dựng nhà cửa. Trong quá trình khai thác dầu, axit clohydric có thể được bơm vào quá trình hình thành đá của giếng dầu để hòa tan một phần của đá, còn được gọi là “xả”, tạo thành các lỗ rỗng lớn hơn.
Thận trọng khi sử dụng và bảo quản axit clohydric

Cách sử dụng và bảo quản HCL Khi sử dụng Axit Clohidric:
-
- Khi tiếp xúc trực tiếp với axit clohydric, chúng ta cần trang bị đầy đủ thiết bị bảo hộ như găng tay cao su, khẩu trang hoặc mặt nạ phòng độc, kính bảo hộ …
- Tránh hóa chất nếu xảy ra tràn, hãy rửa ngay khu vực bị đổ axit clohydric bằng nước.
- Khi bị tạt axit clohydric, phải rửa ngay bằng nước nhiều lần cho đến khi hết ngứa hoặc bay vào mắt thì phải đưa đến cơ sở y tế để điều trị.
Bảo quản axit clohydric:
-
- Bảo quản axit ở nơi khô ráo, thoáng mát, tránh ánh nắng trực tiếp và mưa.
- Nhà kho cần thực hiện các bước để tránh nguy cơ bị đổ. Vết nứt, rò rỉ axit
- Sàn kho phải làm bằng vật liệu chịu axit
- Không bao giờ bảo quản chung với các chất dễ cháy, dễ oxy hóa (đặc biệt là axit nitric hno3 và các hợp chất clorat).
- Không để axit tiếp xúc với kim loại.
Tham khảo thêm các bài viết khác của trung son: Potassium Iodide là gì? Thận trọng khi dùng kali iodua
Tôi có thể mua axit clohydric chất lượng cao ở đâu

HÓA chất HCL àm trung sơn cung cấp Nếu bạn đang muốn tìm mua sản phẩm Axit Clohidric trên thị trường thì đừng nên bỏ qua Công ty TRUNG SƠN. Chúng tôi là một trong những địa chỉ tin cậy chuyên cung cấp các loại hóa chất công nghiệp, hóa chất tinh khiết uy tín.
Bạn sẽ không tìm thấy ở đâu như công ty chúng tôi với các sản phẩm chất lượng và nguồn uy tín. Ngoài ra, bạn sẽ nhận được sự tư vấn nhiệt tình từ đội ngũ nhân viên tay nghề cao và vô cùng nhiệt tình.
Có thể sau khi đọc bài viết này của Zhongshan, bạn đã trả lời được câu hỏi ở đầu bài như axit clohiđric là gì? Axit clohydric có cấu trúc phân tử như vậy. Có nó? Axit clohydric có những tính chất hóa lý nào? Axit clohiđric được điều chế như thế nào? Và ứng dụng nổi bật của axit clohiđric và cách sử dụng, bảo quản đúng cách?
Mọi thắc mắc hoặc muốn mua sản phẩm vui lòng liên hệ trực tiếp trên website trung son hoặc comment bên dưới bài viết này để được nhân viên hỗ trợ.
Liên hệ với chúng tôi qua hotline: (028) 3811 9991 để được hỗ trợ – tư vấn nhanh nhất
Nguồn: https://xettuyentrungcap.edu.vn
Danh mục: Hỏi Đáp