Sự điện li là gì? Độ điện li là gì? Phân loại chất điện ly mạnh yếu?
Kiến thức về chất điện ly sẽ giúp các em học sinh nắm vững các dạng toán và bài tập. Hãy cùng tác giả tìm hiểu điện phân là gì? chất điện giải là gì? Thế nào là chất điện li mạnh và yếu? Bỏ túi lý thuyết hay trong bài viết này
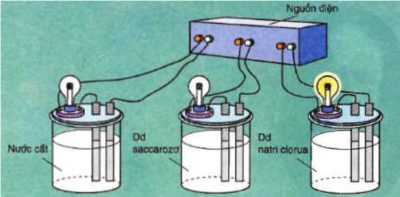
1. Hiện tượng điện li:
Khi nối các dây dẫn vào cùng một nguồn điện ta chỉ nhìn thấy bóng đèn trong cốc đựng dung dịch xà phòng. Vì vậy, dung dịch nacl dẫn điện, nhưng nước cất và dung dịch sucrose thì không.

Nếu làm thí nghiệm tương tự ta sẽ thấy: Natri clorua rắn, khan;
Ngược lại, dung dịch axit, bazơ, muối đều dẫn điện.
Lý do:
– Ngay từ năm 1887, areeni-ut (s.arrhenius) đã công nhận và sau đó được thực nghiệm xác nhận:
– Dung dịch axit, bazơ, muối dẫn điện do trong dung dịch của chúng có các hạt mang điện chuyển động tự do gọi là ion.
– Điện phân là quá trình các chất trong nước phân li thành ion. Các chất tan trong nước phân li thành ion gọi là chất điện li.
2. Điện phân là gì?
– Chất điện ly: là chất tạo thành dung dịch dẫn điện khi hòa tan trong nước.
– Sự điện li: là quá trình phân huỷ các chất trong nước thành ion. Các chất phân li thành ion khi tan trong nước gọi là chất điện li.
– Chất điện li gồm: axit, bazơ và muối
– Sự điện ly được biểu diễn bằng phương trình điện ly. Ví dụ:
nacl → na+ + cl-
hno3 → h+ + no3-
naoh → na+ + oh-
3.Chất điện phân là gì?
– Để biểu thị mức độ phân li ion của chất điện li, ta dùng khái niệm độ điện li
+ Độ phân ly α (alpha) của chất điện li là tỉ số giữa số phân tử phân li thành ion (n) trên tổng số phân tử bị hoà tan (không).
Ta có 0 α ≤ 1 hoặc 0% α 100%
Không điện ly nghĩa là không phân ly: α = 0
Chất điện ly mạnh, phân ly hoàn toàn: α = 1 hoặc 100%
Chất điện ly yếu, phân ly không hoàn toàn 0 <; α < 1
Vậy có thể nói một cách khác: ở cùng nhiệt độ và cùng nồng độ mol/l, chất điện li càng mạnh thì độ phân li α càng lớn.
+ Tỉ lệ mol cũng là tỉ lệ mol nên α bằng tỉ lệ giữa phần mol chất tan đã phân li thành cp và tổng nồng độ mol ct của chất tan trong dung dịch:
Biểu thức:
Trong đó: n là số phân tử bị phân ly thành ion và no là số phân tử bị hòa tan.
clà nồng độ mol của chất tan đã phân ly thành ion, và co là nồng độ mol của chất tan.
Chất điện ly α phụ thuộc vào:
– Bản chất của chất tan.
– Bản chất của dung môi.
– nhiệt độ
– Nồng độ chất điện giải.
4. Phân loại chất điện li mạnh, yếu:
4.1. Khả năng đảo ngược chất điện giải:
Khái niệm: Chuyển động của các cation và anion bị mất trật tự nên chúng có thể va chạm và kết hợp lại với nhau để tạo thành phân tử nên ta nói sự phân ly thuận nghịch và phương trình điện ly có thể là phương trình thuận nghịch.
4.2. Chất điện ly mạnh-Chất điện ly yếu:
Chất điện ly mạnh: là chất khi hòa tan trong nước sẽ phân ly các phân tử hòa tan thành ion.
Ví dụ:
– Axit mạnh như hcl, hno3, h2so4…
– Các bazơ mạnh như naoh, koh, ba(oh)2, ca(oh)2…
– Các muối axit mạnh, bazơ mạnh như nacl, kno3, kcl, k2so4
Khi pha loãng, chúng gần như hoàn toàn là chất điện ly, ta nói chúng là chất điện ly mạnh và phương trình phân ly của chúng là bất thuận nghịch. na2so4 → 2na+ + so42-
Chất điện ly yếu: là chất khi tan trong nước chỉ phân ly một phần phân tử hòa tan thành ion, phần còn lại ở dạng phân tử.
Ví dụ:
– Axit yếu như axit hữu cơ, axit hf, axit clohydric, cation nh4+…
– Bazơ yếu như nh3, amin r-nh2…
Xem Thêm : Tuổi Kỷ Dậu sinh năm 1969 mệnh gì, hợp màu gì, hướng nào tốt?
Phương trình điện phân của chúng là phương trình thuận nghịch
Cân bằng điện giải:
Dĩ nhiên phương trình nghịch đảo trên ở trạng thái cân bằng, gọi là cân bằng tự do.
– Cân bằng điện giải cũng là cân bằng nội môi, nên theo le chatelier, cân bằng sẽ chuyển dịch theo chiều ngược lại với chiều thay đổi của cân bằng.
– Sự phân li càng hoàn toàn khi cân bằng chuyển dịch sang phải, sự chuyển dịch cân bằng phụ thuộc vào nhiệt độ, nồng độ mol chất tan.
– Nhiệt độ càng cao, dung dịch càng loãng thì sự phân li càng hoàn toàn và cân bằng càng chuyển dịch sang phải. Vì vậy chúng ta phải so sánh độ bền của các chất điện ly trong cùng điều kiện nhiệt độ và nồng độ.
Ở cùng nhiệt độ và cùng nồng độ mol/l, chất điện li càng mạnh thì phân li càng hoàn toàn, tức là cân bằng càng chuyển dịch sang phải và ngược lại, chất điện li càng yếu thì phân li càng kém , cân bằng càng chuyển dịch theo chiều nghịch nhiều hơn.
5.Các dạng bài tập về điện li:
Dạng 1: Bài tập Lý thuyết chất điện li, Chất điện li, Viết phương trình chất điện li
Ví dụ, nếu bạn pha loãng dần dung dịch axit sunfuric, bạn sẽ thấy rằng độ dẫn điện của dung dịch lúc đầu tăng lên rồi sau đó giảm xuống. Hãy giải thích hiện tượng này.
Mô tả:
Axit sunfuric phân ly như sau:
h2so4 → h+ + hso4- : điện li hoàn toàn.
hso4- h+ + so42- : k = 10-2
Việc tăng nồng độ chất điện phân sẽ làm tăng nồng độ ion khi bắt đầu pha loãng dung dịch. Vì vậy độ dẫn điện tăng lên. Ở những dung dịch quá loãng thì coi như điện ly hết, nếu tiếp tục pha loãng nữa thì nồng độ các ion giảm xuống làm giảm độ dẫn điện.
Dạng hai: Phương pháp bảo toàn điện tích để giải các bài toán về chất điện phân
Ví dụ, trong 2 lít dung dịch a chứa 0,2 mol mg2+; x mol fe3+; y mol cl- và 0,45 mol so42-. Cô cạn dung dịch x thu được 79 gam muối khan.
a/Tính giá trị x và y?
b/ Biết rằng để được 1 muối thì phải hòa tan 2 muối vào nước. Tính nồng độ mol/lit của mỗi muối trong a.
Mô tả:
a/ Áp dụng định luật bảo toàn điện tích ta có:
2.0,2 + 3.x = 2.0,45 + y ⇒ 3x – y = 0,5 (1)
Cô cạn dung dịch thu được 79 gam muối khan:
0.2.24 + 56.x + 35.5.y + 0.45.96 = 79 ⇒ 56x + 35.5y = 31 (2)
Từ (1),(2) ta có: x = 0,3 và y = 0,4.
b/ Dung dịch a có 2 muối: fe2(so4)3 và mgcl2
cm(fe2(so4)3) = 0,15 mét; cm(mgcl2) = 0,2 m
Dạng 3: cách tính ph
Ví dụ 1: Hòa tan 4,9 mg h2so4 vào nước để được 1 lít dd. Giá trị ph của dd thu được là:
Mô tả:
nh2so4 = 4,9/98 = 0,05 mol ⇒ cm(h2so4) = 5.10-5/1 = 5.10-5 m
⇒ [h+] = 10-4 m ⇒ ph = -log(10-4) = 4
Ví dụ 2: Cho 15 ml dung dịch axit nitric ở ph = 2 trung hòa hết 10 ml dung dịch ba(oh)2 ở ph = a. Giá trị của a là:
Mô tả:
nhno3 = 1,5.10-2.10-2 = 1,5.10-4 ⇒ nba(oh)2 = 7,5.10-5 mol
⇒ cm(oh-) = 1,5.10-4/10-2 = 1,5.10-2 ⇒ poh = 1,8 ⇒ ph = 12,2
Bảng 4: Các dạng bài tập điện phân
Ví dụ 1: Tính nồng độ mol của các ion ch3cooh, ch3coo-, h+ ở trạng thái cân bằng trong dung dịch ch3cooh 0,1M, α = 1,32%.
Mô tả:
ch3cooh : h+ + ch3cooh-
Ban đầu c0 0 0
phản hồi c0. α c0 . α c0 . chữ cái
Cân bằng c0 .(1- α) c0 . α c0 . chữ cái
Vậy [h+] = [ch3coo-] = c0. α = 0,1. 1,32.10-2 mét=1,32.10-3 mét
[ch3cooh] = 0,1m – 0,00132m =0,09868m
Xem Thêm : Hình ảnh đất nước Việt Nam hình chữ S – cho thuê xe
Ví dụ 2: Một dung dịch chứa các ion: mg2+, cl-, br-.
– Nếu cho dd này phản ứng với dd HCl dư thu được 11,6g kết tủa.
– Nếu cho dd này phản ứng với agno3 thì cần nạp đúng 200ml agno3 2,5M, sau phản ứng thu được 85,1g kết tủa.
a. Tính [ion] trong dd đầu? Biết rằng vdd = 2 lít.
b.Cô cạn dung dịch ban đầu thì thu được bao nhiêu gam chất rắn?
Mô tả:
Phương trình ion: mg2+ + 2oh- → mg(oh)2↓
0,2 0,2 nốt ruồi
ag+ + cl- → agcl↓; ag+ + br- → agbr↓
Gọi x, y là số mol của cl-, br-.
x + y = 0,5 (1) ; 143,5x + 188y = 85,1 (2) . Từ (1),(2) x = 0,2, y = 0,3
a. [mg2+] = 0,2/2 = 0,1 m; [cl-] = 0,2/2 = 0,1 m; [br-] = 0,3/0,2 = 0,15 m
b. m = 0,2.24 + 0,2.35,5 + 0,3.80 = 35,9 gam.
Dạng 5: Dạng Động Học Của Phản Ứng Trao Đổi Ion Trong Dung Dịch
Ví dụ: dd x chứa các ion: fe3+, so42-, nh4+, cl-. Chia dd x thành 2 phần bằng nhau:
Phần 1: Phản ứng với nah dư, đun nóng thu được 0,672 lít khí (đktc) và 1,07 gam kết tủa.
Phần II: Phản ứng với dd bacl2 dư thu được 4,66g kết tủa. Tổng khối lượng dd x muối khan thu được khi cô cạn nước là (ở hơi nước chỉ có nước bay hơi)
Mô tả:
nnh4+ = nnh3 = 0,672/22,4 = 0,03 mol
nfe3+ = 1,07/107 = 0,01 mol; nso42- = 4,66/233 = 0,02 mol
Áp dụng nguyên tắc bảo toàn điện tích: 3.0,01 + 0,03 = 2.0,02 +x ⇒ x = 0,02
Mét = 0,01,56 + 0,03,18 + 0,02,96 + 0,02.35,5 = 3,73 gam
Khối lượng x muối khan trong dung dịch: 3,73,2 = 7,46 gam
Dạng 6: Phản ứng thủy phân muối
Giải thích môi trường dung dịch muối: fe2(so4)3; khso4; nahco3; k2s; ba(no3)2; ch3cook.
Mô tả:
+ fe2(so4)3 → 2fe3+ + 3so42-
fe3+ + h2o fe(oh)2+ + h+
⇒ môi trường axit
+ khso4 → k+ + hso4-
hso4- + h2o ⇔ so42- + h3o+
⇒ môi trường axit
+ nahco3 → na+ + hco3-
hco3- + h2o co32- + h3o+
hco3- + h2o h2co3 + ồ-
⇒ môi trường trung tính
+ k2s → 2k+ + s2-
s2- + h2o hs- + oh-
⇒ Môi trường cơ bản
+ ba(no3)2 → ba2+ + 2no3-
⇒ môi trường trung tính
+ ch3cook → ch3coo- + k+
ch3coo- + h2o ch3cooh + oh-
⇒ Môi trường cơ bản.
Nguồn: https://xettuyentrungcap.edu.vn
Danh mục: Hỏi Đáp
